El agua de mar

Cuál es el origen del agua salada, su composición e importancia para el acuario marino. Tras haber leído el número anterior de esta revista, podemos hacernos a la idea de los principios químicos del agua. Pero posiblemente una de las preguntas que alguna vez nos hemos hecho todos, ¿por qué el agua de mar es salada? Pues comenzaremos por el principio.
Origen del agua salada
Hace aproximadamente 4650 millones de años el planeta Tierra era una gran masa caliente en la que no podríamos diferenciar mares, océanos y tierra. Cuando esta masa caliente se fue enfriando empezaron a expulsarse del interior de la corteza terrestre una gran cantidad de gases, entre ellos vapor de agua, que con el tiempo se condensó, dando lugar a la formación de mares y océanos, pero en aquel momento toda aquella agua no era precisamente salada, si no más bien dulce.
Y ¿cómo se convirtió el agua dulce en salada? Pues a medida que los continentes se formaban, las constantes lluvias iban arrastrando y disolviendo una gran cantidad de sales de la superficie terrestre, principalmente Cloruro de Sodio junto a otros compuestos químicos como Carbonatos y Bromuros entre otros. Pero no todas las sales era arrastradas desde la superficie, una gran cantidad se disolvía directamente del fondo oceánico y también eran expulsadas directamente por erupciones subacuáticas. Si tenemos en cuenta este proceso de salinización, podremos observar que se trata de un ciclo ininterrumpido que en la actualidad sigue llevándose a cabo, ya que, la erosión de los ríos y torrentes el lixiviado ocasionado por las lluvias, provocan la eliminación de las sales de la corteza de los continentes que es finalmente depositada en su gran mayoría en mares y océanos.
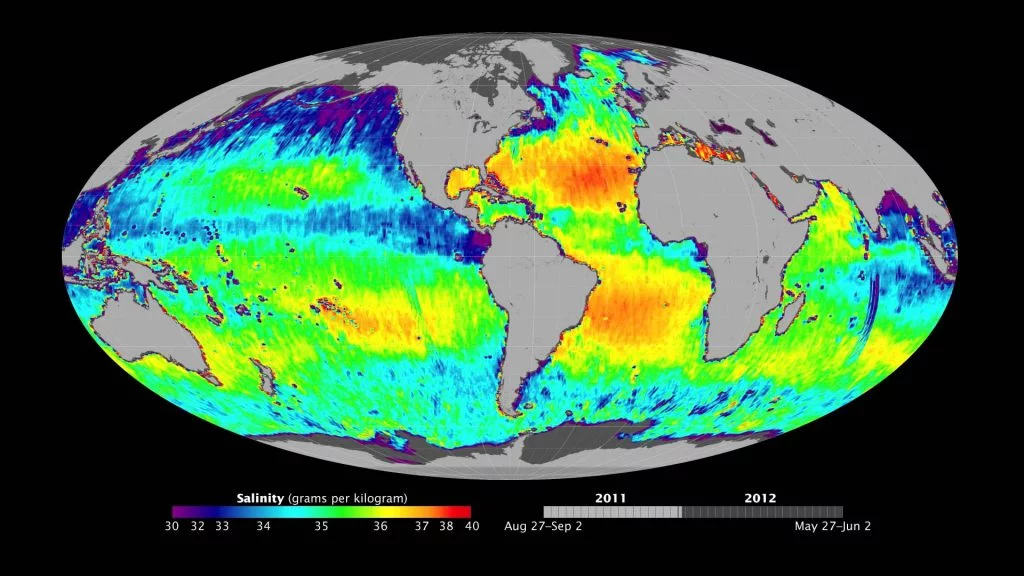
Otra gran cuestión, es por qué no todos los mares poseen la misma salinidad. Existen distintos parámetros físicos que dan lugar a estas diferencias. Desde la temperatura de la superficie del océano, las corrientes marinas o el aporte de agua dulce por: intensas lluvias, el derretimiento de los polos o por ríos. Debido a estas modificaciones fisicoquímicas podemos ver por ejemplo, que la salinidad en los polos es más baja que en el océano Atlántico y éste a su vez es menos salino que el mar Mediterráneo.
Composición del agua salada
Pues muy bien, una vez conocido el origen de las sales de nuestros mares, debemos saber cuáles son los principales elementos que la componen.
Pero para ello necesitamos conocer cómo se comporta una sal ante un disolvente polar (agua en este caso). Las sales son compuestos iónicos que como su nombre indica, están formados por iones positivos (Cationes) y negativos (Aniones).
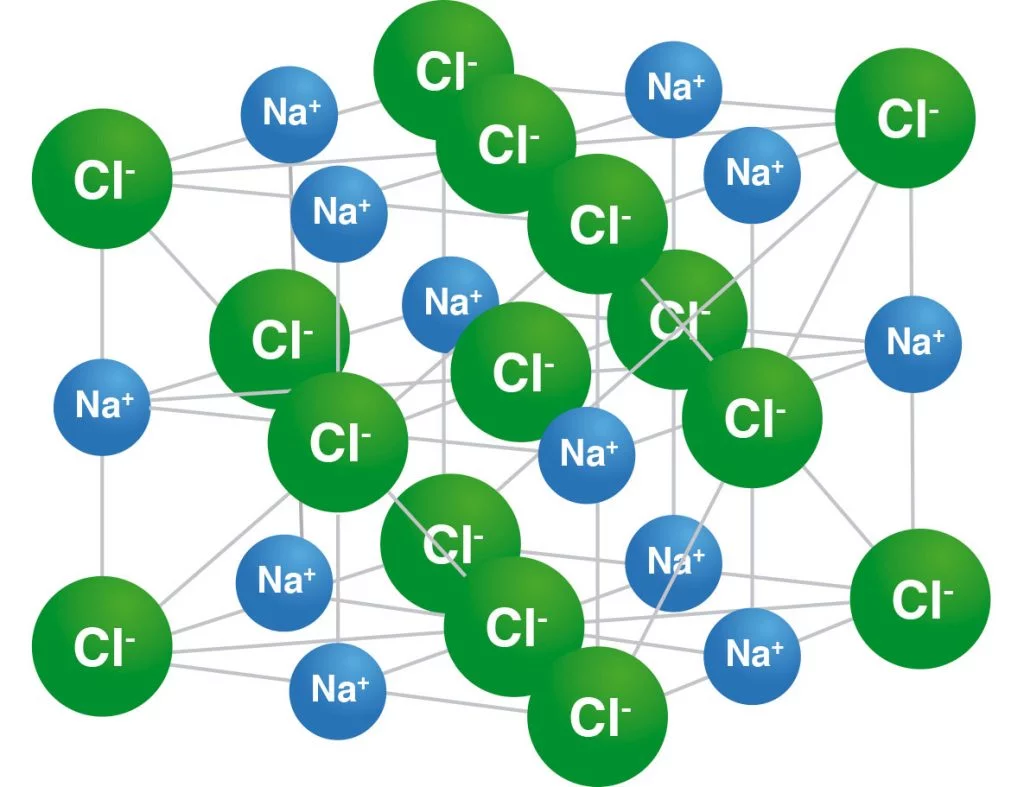
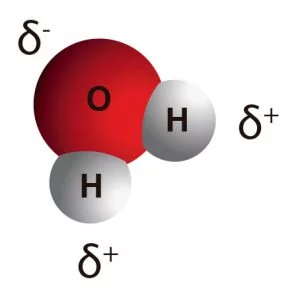
En una sal las cargas positivas y negativas son equivalentes entre si, de este modo se puede mantener la estabilidad y neutralidad de la molécula. Por otro lado encontramos un disolvente que es el agua. La molécula de agua es covalente y aunque es una molécula muy estable, posee unas cargas parciales, lo que le permite poseer polaridad y proporcionas las capacidades como solvente.
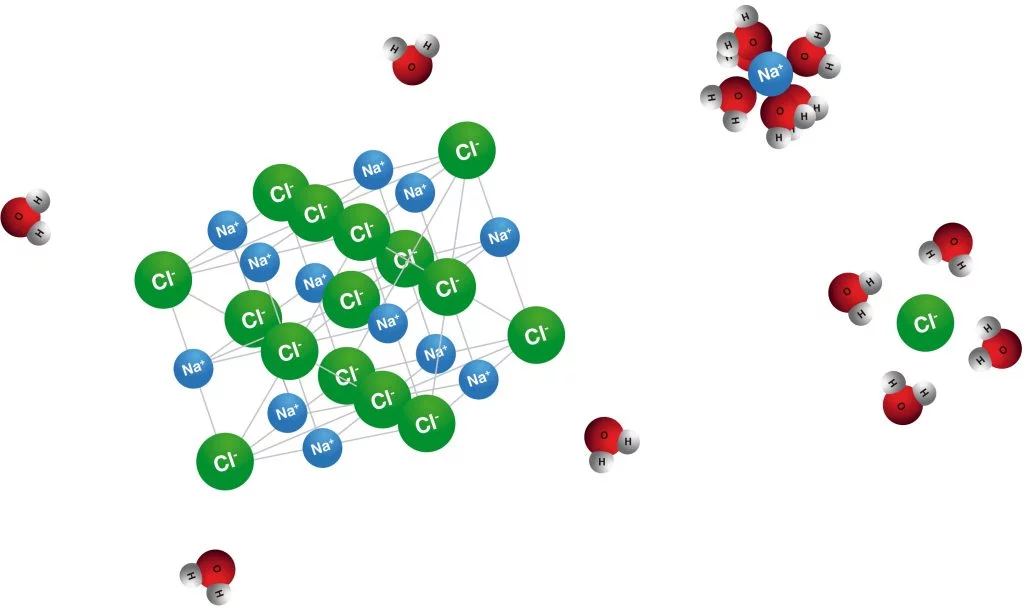
Ahora bien, si juntamos una sal como el Cloruro de Sodio o sal común con agua, los cationes de Sodio son rodeados por los polos negativos de la molécula de agua, y los polos positivos rodean a los aniones de la sal disolviendo la estructura salina en el agua. Pero no todos los compuestos iónicos pueden disolverse en agua, esto dependerá la fuerza de atracción entre sus iones. Por ejemplo el carbonato cálcico o aragonito (CaCO3), es muy estable y difícil de disolver en agua.
Tras esta breve descripción del proceso físico-químico de la disolución de las sales, los principales iones que se encuentran en el agua de mar son los siguientes:
Al final de esta tabla observamos el término de salinidad total que equivale aproximadamente a 35 g/L, que quiere decir que existen aproximadamente 35 gramos de sal por cada litro de agua de mar. Pero, ¿qué unidades existen para medir la salinidad? Pues podemos encontrar tres escalas principales: la densidad (ρ), la conductividad o concentración (gramos/litro).
La densisdad (ρ)
Es la masa (m) de un compuesto por unidad de volumen (v). Por lo que si una muestra de agua de mar tiene una gravedad específica de 1023 quiere decir que su masa es de 1023 gramos por cada litro de su propio volumen.
ρ=m/v
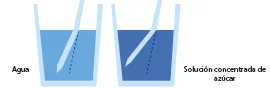
Para medir la densidad en un acuario podemos utilizar un densímetro que mediante su flotabilidad y una escala nos señala la densidad del agua del acuario; o un refractómetro, que nos proporciona la densidad de un fluido gracias a las propiedades físicas del mismo, funcionando de la siguiente manera.
En función de la densidad de un fluido el ángulo de refracción de la luz varía, tal como se observa en la ilustración. Por lo que si se calibra un aparato con una escala se puede utilizar este proceso físico para determinar la densidad de un fluido.

La conductividad o concentración (gramos/litro)
La conductividad del agua es la inversa de la resistencia que opone el agua al paso de una corriente eléctrica y se mide en micro Siemens/cm (µS/cm). Este valor se puede medir mediante un conductímetro, este aparato aplica un campo eléctrico entre dos electrodos separados una distancia determinada entre si, midiendo la resistencia eléctrica de la disolución.
Debemos saber que mayor contenido de iones en la disolución mayor será la conductividad, por lo que el agua salada posee una mayor conductividad que el agua dulce.
La concentración de sales
Medir la concentración es una tarea compleja puesto que deberíamos evaporar el agua por completo para poder tomar esta medición por lo que se utilizan una serie de relaciones con los dos parámetros anteriores. Si queremos pasar de Conductividad a Concentración multiplicaremos el valor obtenido en µS por 0.64 que es una constante, mientras que para pasar de densidad a concentración la fórmula es algo más compleja:
S = 0.03 + 1,805 * (1.1/1.47+ ρ’/1.47)
En el valor de ρ^’ debemos insertar las dos últimas cifras del valor de la densidad. Es decir si la densidad es de 1023, pondremos 23.
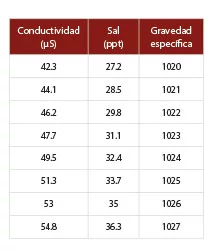
Pero si no queremos andar con fórmulas siempre podremos utilizar la siguiente tabla de equivalencias:
Tras esta explicación ya sabemos que el agua de mar está cargada de iones, siendo los de Sodio y Cloruro los más abundantes. Pero no por ello el resto de iones son menos importantes, de hecho en el acuario marino existen determinados iones que nos asegurarán la buena salud del mismo. Un parámetro que todos tenemos en cuenta pero que muchos no tienen claro de que se trata es el KH. El KH es un parámetro que determina la dureza de carbonatos del agua. Este valor permite mantener un pH estable en nuestro acuario, evitando variaciones bruscas (efecto tampón), y por otra parte valores elevados de entre 7 y 10 unidades, ayudarán a mantener una cantidad de iones de Calcio suficientes para que sean fijados por organismos con conchas o esqueletos calcáreos, como corales, algas coralinas o diversos moluscos. No debemos confundir el KH con el GH que mide las concentraciones de iones de Calcio y Magnesio disueltos en el agua.
¿Por qué hablamos de carbonatos, de Calcio y de Magnesio? Pues entre ellos existen relaciones muy directas. En primer lugar sus sales serían Carbonato cálcico y magnésico, que al disolverse forman esos tres iones que son de gran importancia en el equilibrio de nuestro acuario. Todos pensamos que los valores del calcio con muy importantes y debemos mantenerlos entre 400 y 450mg/L, y es cierto pero posiblemente el Magnesio sea más importante ya que, de los niveles de este ion en el acuario, dependen los niveles de Calcio. Esto se debe a que, cuando los valores de Magnesio están por debajo de 1200mg/L los iones de Calcio precipitan y no son asimilables por los organismos del acuario. Y del mismo modo, si los valores de Calcio son muy bajos el Magnesio precipitaría, en ambos casos en forma de carbonatos.
Como hemos podido comprobar el agua de mar es una sopa compleja de diferentes iones que de forma natural intentan mantener un equilibrio entre ellos, viéndose afectados en su totalidad al añadir o eliminar alguno de ellos.
Por eso es tan importante la sal utilizada en nuestro acuario. Y no solo la sal, si no los niveles de los parámetros más relevantes como el KH que ayudará a mantener un pH estable y una buena relación de Calcio y Magnesio, que permitirá a nuestros corales crecer sanos y con menos complicaciones.
agua de mar, agua marina, agua salada, composición, origen, parámetros